|

Le graphite, une forme allotropique du carbone
Bien que composant fondamental de la vie sur Terre, le carbone ne représente que 0,048 % de la croûte terrestre! Les formes principales naturelles du carbone sont le carbone amorphe (structure non cristalline), le graphite, le diamant, plus rarement la lonsdaléite et encore plus rarement les fullérènes et les nano-tubes. La différence entre ces formes cristallines dites allotropiques proviennent de la façon dont sont reliés les atomes de carbone entre eux, créant des configurations géométriques différentes.
En ce qui concerne le graphite, il peut cristaliser sous une forme rhombaédrique ou une forme hexagonale : seule cette dernière est stable, le cristal étant constitué d'un empilement de couche d'atomes formant un réseau en "nid d'abeille", chacun relié à ses 3 voisins les plus proches par une liaison covalente forte de type sigma. Le graphite est anisotrope, ses propriétes physiques dépendent de la direction considérée. Par exemple, les différentes couches, séparé par une distance de 0,336 nano-mètres, peuvent facilement glisser les unes sur les autres.
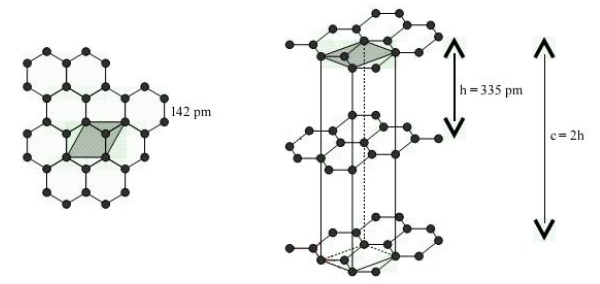
Par comparaison, le diamant a une structure cristalline tétraédrique, chaque atome étant reliés à 4 autres atomes par une liaison covalente forte. Le diamant est isotroprique et est un matériau très dur. Cependant comme le montre le diagramme simplifiée des phases du carbone ci-dessous, pour les valeurs de température et de pression ambiantes, le diamant est dans un état méta-stable, destiné à se transformer en graphite ou en carbone amorphe : toutefois, ce processus est très lent même à l'échelle géologique!
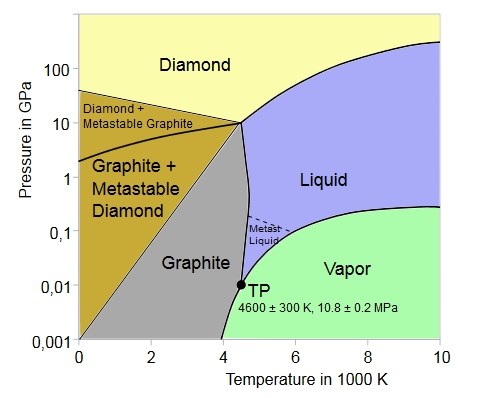
Le graphite est un élément présent naturellement dans la croute terrestre, issu des processus métamorphiques, la structure cristalline pouvant apparaître en fonction de la pression, en général au delà de 650-700 degrés celsius, à partir des atomes de carbones résultant de la transformation de roches ou de composés organiques (graphitisation). Au Chardonnet, le graphite provient probablement de la transofmation des grès à anthracite au contact du porphyre dioritique.

Propriétés physiques du graphite
Le graphite est un matériau sombre avec des reflets métalliques, le diamant étant lui translucide. Sa dureté est faible, entre 1 et 2 sur l'échelle de Mohs : il peut être rayé par l'ongle. Par comparaison, le diamant est au niveau 10, le plus haut de cette échelle et la lonsdaléite est théoriquement encore plus dure. Le graphite est relativement léger avec une densité comprise entre 2 et 2,3 g/cm3 (par comparaison, le diamant dépasse 3,5 et le granite 2,6). Alors que le diamant est un très bon isolant, les électrons du graphite laissés libres par la quatrième liaison entraînent une bonne conductivité dans les plans des empilements de couches; c'est un semi-métal. En isolant une couche de graphite, on obtient un nouveau matériau le graphène qui est encore plus conducteur que le graphite et est aussi un exceptionnel conducteur de chaleur, en plus d'avoir une résistance à la rupture plus importante que l'acier. Dans certaines directions, le graphite est lui aussi un bon conducteur de chaleur. De densité faible, le graphite résiste bien à la traction et la compression et est stable thermiquement et chimiquement.

Utilisations du graphite
A cause de ses caractéristiques et chimique, le graphite a des utilisations nombreuses et variées:
- les mines de crayons. Il s'agit d'un de ses premiers usages et est à l'origine de son nom moderne (le graphite s'appelait autrefois plombagine, en l'associant à tord au mine de plomb utilisée pour écrire à l'époque). Mélangé à de l'argile en diverses proportions, il permet d'obtenir des mines de duretés et de rendus graphiques différents (de H pour les mines dures à B pour les mines grasses en passant par les mines HB standard).
- les creusets. En vertu de sa forte résistance thermique, le graphite peut être utilisé pour confectionner des moules et creusets à métaux. Au XVIème siècle le roi d'Angleterre s'appropria une des premières mines de graphite pour l'utiliser dans la fabrication de boulets de canon plus performants.
- les lubrifiants sec qui utilisent directement les propriétés de glissement des couches de graphites entre elles.
- les anodes de batteries, notamment lithium-ion, une voiture électrique pouvant nécessiter plusieurs dizaines de kilos de graphite.
- les charbons et balais des moteurs and dynamos.
- la production de fonte et d'acier en tant que réducteur.
- les plaquettes de frein.
- les électrodes.
Le demande en graphite de bonne qualité est donc en croissance au niveau mondial. La Chine dispose de la majorité des réserves et contrôle actuellement 80% de la production.
La mine de graphite du Chardonnet
Située à environ 2700 mètres d'altitude, cette mine a fait l'objet d'une concession royale le 10 mars 1824. Ce n'est qu'au début du XXème siècle que l'exploitation a réellement pris son essort, en surmontant les freins dues à l'éloignement (les mineurs passaient une semaine entière dans la montagne) et aux difficiles conditions d'extraction en altitude. En effet, la principale mine européenne étant allemande, des investissements furent réalisés pour la seule mine industrielle en France (raccordement au réseau électrique coté Clarée, perforatrices, wagonnets, téléphérique de 4 kilomètres coté Guisanne). Avec les difficultés d'approvionnement en provenance de Madagascar pendant la Première Guerre Mondiale, la production de la mine s'accrut jusqu'à atteindre un maximum de 2132 tonnes pour l'année 1918. La paix revenue, la production décrut progressivement jusqu'à l'arrêt de l'exploitation en 1930.

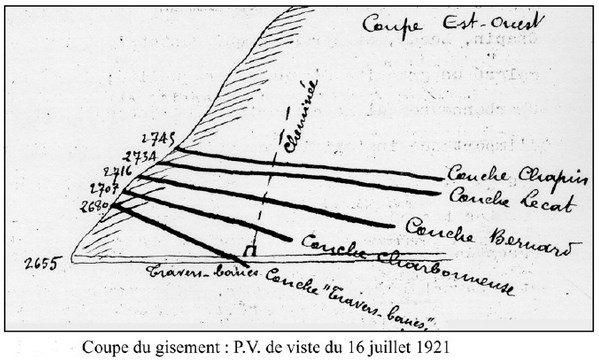
Sous l'impulsion d'archéologues et géologues, notamment dans l'association Société Géologique et Minière du Briançonnais, la mémoire des mines d'altitude de la région est conservée et les collectivités locales ont réalisé quelques aménagements pour conserver cet intéressant patrimoine (installation d'une grille pour éviter la condamnation de la mine par éboulement de l'entrée du travers-banc, stabilisation du chevalet du téléphérique qui est emblématique de cette mine).
 
 
Condition d'accès au site
Les ruines de la mine sont en montagne, accessibles par une randonnée de plusieurs heures avec environ 900m de dénivellé, à partir de la vallée de la Guisane (parking du Pont de l'Alpe, 1710 mètres) ou de la Clarée (parking de Fontcouverte, 1850 mètres). Des géocaches matérielles sont présentes sur les deux itinéraires. L'entrée de la mine est située dans la pente détritique faisant face au massif de l'Oisan, au nord du col du Chardonnet, le long du sentier vers les cols des Béraudes et de la Ponsonnière. Une grille en protège l'accès mais elle n'est pas cadenassée. Pendant l'approche finale, attention aux chutes de rochers et aux glissades sur le pierrier ou la neige!
 
Validation de la cache
Pour valider la cache vous devez envoyer les informations suivantes (vous pouvez en parallèle publier votre visite sans attendre la réponse):
- Décrivez la nature du sol (couleurs, consistance, structure...) quelques mètres après l'entrée de la mine (ne pas aller au delà, les galeries secondaires n'étant pas sûres d'après une étude du BRGM).
- Citez un matériau moins dur que le graphite.
- Expliquez pourquoi les diamants ne sont pas éternels, contrairement au graphite.
- Citez l'application du graphite qui en fit un élément stratégique pour les militaires.
- Prenez une pierre sombre dans la mine ou les détritus en dessous et indiquez quels tests vous avez faits pour déterminer s'il s'agissait de graphite.
En prime, si vous le pouvez, merci de prendre en photo le splendide panorama visible depuis l'entrée de la mine et de publier dans votre log le reportage photographique de votre randonnée.
|