Dmitrij Ivanovic
Mendelejev

(27. ledna (8.února) 1834, Tobolsk – 20. ledna (2.února)
1907, Petrohrad, byl ruský chemik a tvurce periodické tabulky
prvku.
Mendelejev je objevitelem periodického zákona prvku z roku 1869.
Mendelejev publikoval svou první tabulku prvku v casopise Ruské
chemické spolecnosti v roce 1869, o rok pozdeji pak predložil
tabulku presnejší, doplnenou o další prvky. Práce z
roku 1870 mela název Prirozená soustava prvku a její
použití k udání vlastností prvku dosud neobjevených.

K nejslavnejším objevum predpovezených prvku patril objev
eka-aluminia (Ga), eka-boru (Sc) a zejména eka-silicia (Ge),
jehož vlastnostem Mendelejev venoval nejvíce pozornosti.
Gallium objevil v roce 1875 Lécoq de Boisbaudran spektrální
analýzou ve sfaleritu, skandium roku 1879 Lars Frederik Nilson pri
studiu sloucenin prvku vzácných zemin a germanium roku 1886 Clemens
Winkler pri analýze nerostu argyroditu. Objev germania se stal
triumfem objevu periodického zákona.
Geniálnost Mendelejevova usporádání prvku, které je projevem
pochopení prirozeného vztahu mezi prvky, potvrdilo studium
rentgenových spekter a kvantová mechanika. Jen v puvodní formulaci
periodického zákona došlo ke zmene: výraz „atomová
váha“ byl nahrazen výrazem atomové (nyní protonové) císlo.
Podnetem k tomu byly výzkumy radioaktivity a rentgenových spekter,
pri nichž zjistil britský fyzik Henry Gwyn Jeffreys Moseley
vztah mezi vlnoctem spektrální cáry K-série rentgenového spektra a
poradovým císlem prvku v periodické soustave.
Mendelejev publikoval na 400 prací (vcetne prací z fyziky a
metrologie), napr. práce o puvodu ropy a o jejím prumyslovém
zpracování, o roztocích, provedl také napríklad predbežné
výpocty ledoborec Jermak. Napsal vynikající ucebnici Základy
chemie. Roku 1868 pomohl založit Ruskou chemickou
spolecnost a roku 1906, pár mesícu pred svou smrtí, bohužel
nezískal Nobelovu cenu za chemii o pouhý jeden jediný hlas.
Mendelejevovým jménem je nazván kráter na Mesíci, minerál
mendelevit a 101. prvek mendelevium.

Historie tabulky
1789 - Antoine Laurent Lavoisier (1743-1794)-
v "Pojednání o základech chemie" rozdelil prvky podle
fyzikálních a chemických vlastností na kovy a nekovy (v té
dobe známo cca 40 prvku). Již predtím v roce 1774 zformuloval
zákon o zachování hmoty a definitivne tak vyvrátil teorii
flogistonu a v roce 1787 vydal spis o chemickém názvosloví.
1818 - Jöns Jacob Berzelius (1779 - 1848)
Významne zdokonalil chemické názvosloví a symboliku. Daltonovy
znakové symboly prvku nahradil písmenovými symboly, které
používáme dodnes. Zabýval se katalýzou, isomerií, izomorfií
(zavedl pojem alotropie a oznacení mer). Pro svou slucovací teorii
využil první elektrochemické poznatky. Predpokládal, že
vlastností atomu prvku jsou elektrické náboje. Podle
tohorozdelil prvky na elektropozitivní a elektonegativní, pouze
vodík byl prechodným prvkem
1829 - Johann Wolfgang Döbereiner (1870-1849),
profesor jenské univerzity. Zabýval se mimo jiné studiem vodního
plynu, katalýzou, objevil furfural a formuloval zákon triád
(Li - Na - K, Ca - Sr - Ba, S - Se - Te, Cl - Br -
I) s tím, že fyzikální a chemické vlastnosti mají
prumer ve stredním prvku
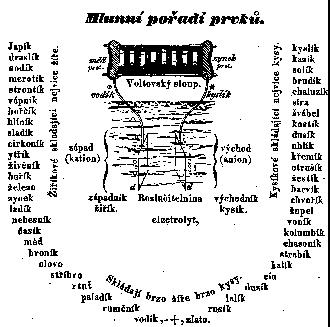
1852 - Karel Slavomil Amerling (1807-1884) v
uvedeném roce publikoval Pictus Orbis (Svet v obrazech), kde bylo
uvedeno tzv. mlunní poradí prvku, kde byli serazeny
prvky (s ceskými originálními názvy), v poradí
dle (dnes bychom rekli)
elektronegativy.
1862 - Alexandre-Emile Béguyer de Chancourtois (1820
– 886) predložil systém všech 62 tehdy
známých chemických prvku serazených pole stoupající atomové
hmotnosti a dal mu trojrozmernou podobu "tellurického
šroubu". Správne však zaradil jen 23 prvku. Zavedl
pojem perioda
1864 - John Alexander Reina Newlands (1838 –1898)
byl anglický analytický chemik, který zavedl ve svém
systému místo "atomových vah" poradová císla prvku a sestavil z
nich první periodickou tabulku, když seradil všech 62
známých prvku po osmi (6 míst však bylo zdvojeno) do sedmi
period. Tvrdil, že jsou-li prvky takto usporádány, jako by se
u nich opakovaly urcité vlastnosti, svým zpusobem se harmonizují -
na každém osmém míste na stupnici. Newlands tento jev nazval
zákonem oktáv a prirovnal usporádání prvku k oktávám na klávesnici
klavíru.
1864 - William Odling (1829-1921).
Velmi dokonalé usporádání, mezi 57 prvky serazenými do
tabulky podle rostoucí "atomové váhy" dokonce uplatnil výjimku v
poradí u telluru a jodu a vynechal volná místa pro dosud neobjevené
prvky.
1869 - Julius Lothar Meyer (1830–1895).
První tabulku zverejnil již v roce 1864, druhá
zdokonalená periodická tabulka z roku 1969 vyšla tiskem
až v roce 1972. Do tabulky zaradil jen 56 prvku.
S objevem nových prvku souviselo i urcování jejich relativních
atomových hmotností a zkoumání jejich typických reakcí. Chemici
zjištovali, že nekteré prvky mají podobné vlastnosti.
Roku 1829 Johann Döbereiner (1780-1849) prednesl svoji teorii o
triádách prvku (skupiny o trech prvcích). Tak napríklad jednu
triádu tvorily kovy lithium, sodík a draslík, které reagují
podobným zpusobem. Ruský chemik Dmitrij Ivanovic Mendelejev
(1834-1907) zjistil, že u prvku serazených podle vzrustající
atomové hmotnosti se pravidelne (periodicky) opakují podobné
vlastnosti. V nekolika prípadech však musel udelat výjimku a
predradit težší prvek lehcímu. Roku 1869 publikoval
Mendelejev poprvé periodický zákon, který tuto závislost vyjadruje,
a periodickou tabulku prvku, která je grafickým vyjádrením
periodického zákona. V tabulce vynechal místa pro prvky, o kterých
predpovedel, že budou objeveny pozdeji.
Dnes je známo, že prvky nejsou usporádány podle relativní
atomové hmotnosti, ale podle stoupajícího protonového císla. To byl
také duvod, proc musel Mendelejev predradit težší prvek
lehcímu. Mendelejevuv periodický zákon však byl zpocátku
prijat se znacným skepticismem a nebyl dlouhou dobu uznáván.
Až s objevením prvku gallia (1875), skandia (1879) a germania
(1886), které Mendelejev predpovedel již v roce 1871, byl
periodický zákon všeobecne prijat.
Dnes má tabulka 115 prvku (prvek se 118 protony byl sice
již objeven, ale naopak prvky 113, 115 a 117 nebyly
ješte izolovány), pricemž o názvech posledních, nove
objevených prvku se vedla dlouhá diskuse. V roce 1997 konecne
šest nových chemických prvku, objevených v letech 1964-1984
dostalo své jméno. Jde o další transurany, prvky s
vyšším protonovým císlem než je císlo uranu
(92), s poradovými císly 104 až 109. Jména jim udelila
Mezinárodní unie pro cistou a aplikovanou chemii (IUPAC).
Nové transurany dostaly názvy ruthefordium (Rf, 104), dubnium
(Db, 105), seaborgium (Sg, 106), bohrium (Bh, 107), hassium (Hs,
108) a meitnerium (Mt, 109). Objeveny byly v USA, v bývalém
Sovetském svazu a v Nemecku.
Americký návrh pojmenovat prvek císlo 104 po objeviteli
atomového jádra Britovi siru Ernestu Rutherfordovi (1871-1937)
zvítezil nad ruským protinávrhem dát mu jméno po sovetském jaderném
fyzikovi Igoru Kurcatovovi (1903-1960). Na oplátku byl prvek císlo
105 pojmenován po ruském stredisku jaderného výzkumu v Dubne.
Další prvek, císlo 106, nese jméno amerického nositele
Nobelovy ceny Glenna T. Seaborga. Seaborgium je jediným prvkem,
který byl verejne pojmenován po žijící osobe.
Ostatní prvky byly objeveny v letech 1981 až 1984 vedci
Spolecnosti pro výzkum težkých iontu (GSI) v nemeckém
Darmstadtu. Prvek 107 byl pojmenován po dánském nositeli Nobelovy
ceny z roku 1922 Nielsu Bohrovi (1885-1962), prvek 108 nese jméno
spolkové zeme Hesensko, kde Darmstadt leží. Neprošel
návrh pojmenovat ho po Ottovi Hahnovi (1879-1968), nositeli
Nobelovy ceny za rok 1944. Ale ocenen byl neprímo i on: prvek císlo
109 dostal jméno rakousko-švédské fyzicky Lise Meitnerové
(1878-1968), která spolu s Hahnem objevila prvek proaktinium s
protonovým císlem 91 - nejstálejší izotop - a v roce 1933
štepení jader.
Prvky s protonovým císlem 110 a vyšším nejsou v
soucasné dobe ješte pojmenovány a mají prozatímní název a
znacku, které jsou odvozeny podle poctu jejich protonu. Z techto
prvku je pomerne zajímavý prvek s protonovým císlem 114 a
prozatímním názvem ununquadium. Tento nedávno objevený prvek (1998)
má totiž jednu zvláštní vlastnost. Narozdíl od
podobných prvku s vysokým protonovým císlem, které se rozpadají
behem tisícin i milióntin vteriny, má tento prvek polocas rozpadu
kolem triceti vterin. Nejenže to umožní
dukladnejší prozkoumání jeho vlastností, ale vedci se
domnívají, že narazili na tolik ocekávaný "ostrov stability".
Takovéto prvky by pak v budoucnu mohly najít využití v
lékarství ci chemii.
KEŠ NAJDETE NA
SOURADNICÍCH
50° 0 (YPERIT + FOSGEN) (DURAL -
NAFTALEN)
014° 2 (ZIRKON + REPNÝ CUKR) (SMARAGD +
CPAVEK)
Kontrolní soucet císel
celých souradnic je 54.
